Enzimas
Objetivo: Identificará la importancia de la
función que desempeñan las enzimas como catalizadores biológicos.
Lee los apuntes siguientes y desarrolla en tu cuaderno.
Lee los apuntes siguientes y desarrolla en tu cuaderno.
.1 Función de las enzimas
Las enzimas son proteínas que catalizan todas las
reacciones bioquímicas. Además de su importancia como catalizadores biológicos,
tienen muchos usos médicos y comerciales.
Un catalizador es una sustancia que disminuye la
energía de activación de una reacción química. Al disminuir la energía de
activación, se incrementa la velocidad de la reacción.
La mayoría de las reacciones de los sistemas vivos son reversibles, es
decir, que en ellas se establece el equilibrio químico. Por lo tanto, las
enzimas aceleran la formación de equilibrio químico, pero no afectan las
concentraciones finales del equilibrio.
Clasificación de las enzimas
1.- Simples:Formada por una o mas cadena polipeptídica
2.- Conjugadas: Contiene por lo menos un grupo no proteico enlazado a la cadena polipeptídica
Clasificación de las enzimas de acuerdo a su complejidad
De acuerdo a su complejidad y estructura las enzimas se clasifican como:
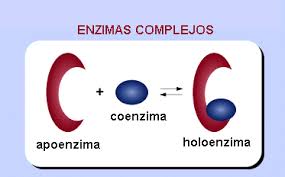
- Apoenzima: Es la
parte polipeptídica de la enzima.
- Cofactor: Es la
parte no proteica de la enzima.
La combinación de la apoenzima y el cofactor forman la holoenzima.
Los cofactores pueden ser:
*Iones metálicos: Favorecen la actividad catalítica general de la
enzima, si no están presentes, la enzima no actúa. Estos iones metálicos se
denominan activadores. Ejemplos: Fe2+, Mg2+, Cu2+, K+, Na+
y Zn2+
*La mayoría de los otros cofactores son coenzimas las
cuales generalmente son compuestos orgánicos de bajo peso
molecular, por ejemplo, las vitaminas del complejo “B” son coenzimas que
se requieren para una respiración celular adecuada.
2.2 Clasificación de las enzimas según su
actividad.-
Tipo de enzimas
|
Actividad
|
Hidrolasas
|
Catalizan reacciones de hidrólisis.
Rompen las biomoléculas con moléculas de agua. A este tipo pertenecen las
enzimas digestivas.
|
Ligasas
|
Catalizan la unión de moléculas.
|
Liasas
|
Catalizan las reacciones de adición de
enlaces o eliminación, para producir dobles enlaces.
|
Oxidorreductasas
|
Catalizan reacciones de óxido-reducción.
Facilitan latransferencia de electrones de una molécula a otra.Ejemplo;
la glucosa, oxidasa cataliza la oxidación de glucosa a ácido glucónico.
|
Tansferasas
|
Catalizan la transferencia de un grupo de
una sustancia a otra. Ejemplo: la transmetilasa es una enzima que
cataliza la transferencia de un grupo metilo de una molécula a otra.
|
3 Actividad enzimática
Los sustratos son específicos para cada enzima:
La sacarosa es el sustrato de la sacarasa que actúa rompiéndola en sus componentes.
La sacarosa es el sustrato de la sacarasa que actúa rompiéndola en sus componentes.
Las enzimas actúan de acuerdo con la siguiente secuencia: La enzima (E) y
el sustrato (S) se combinan para formar un complejo intermedio enzima sustrato (E-S),
el cual se descompone formando un producto y regenerando la enzima.
El grado de especificidad de las enzimas es muy alto, pueden distinguir
incluso entre diferentes tipos de isómeros. Se cree que la especificidad de la
enzima es debido a la forma particular de una pequeña parte conocida como sitio
activo, la cual se fija a la contraparte complementaria en el sustrato.
Actividad:
ACTIVIDAD Nº1:
1.- Dibuje un modelo
de tipo “Cerradura y Llave”.
2.- Dibuje un modelo
de “Ajuste Inducido”.
3.- Define a los componentes de la accion enzimática.
4.-
Las hidrolasas son enzimas presentes en el tracto digestivo principalmente y su
función principal es:
4 Factores que afectan la actividad enzimática.-
Concentración del sustrato.- A
mayor concentración del sustrato, a una concentración fija de la enzima se
obtiene la velocidad máxima. Después de que se alcanza esta velocidad, un
aumento en la concentración del sustrato no tiene efecto en la velocidad de la
reacción.
Concentración de la enzima.- Siempre
y cuando haya sustrato disponible, un aumento en la concentración de la enzima
aumenta la velocidad enzimática hacia cierto límite.
Temperatura.- Un incremento de 10°C
duplica la velocidad de reacción, hasta ciertos límites. El calor es un factor
que desnaturaliza las proteínas por lo tanto si la temperatura se eleva
demasiada, la enzima pierde su actividad.
pH.- El pH óptimo de la actividad enzimática es
7, excepto las enzimas del estómago cuyo pH óptimo es ácido.
Presencia de cofactores.- Muchas
enzimas dependen de los cofactores, sean activadores o coenzimas para funcionar
adecuadamente. Para las enzimas que tienen cofactores, la concentración del
cofactor debe ser igual o mayor que la concentración de la enzima para obtener
una actividad catalítica máxima.
Las enzimas no se alteran ni se consumen, por lo que pueden volver a utilizarse
Cada enzima tiene uno o más sitios activos que se ubican en la superficie de la enzima. Durante la reacción las moléculas de sustrato que ocupan estos sitios quedan mas cerca unas de otras y reaccionan entre sí.
Se han propuesto dos modelos para explicar la unión enzima sustrato, según el modelo llave cerradura podría pensarse en las enzimas como una especie de cerradura molecular en donde entran solo llaves moleculares. Esta situación nos plantea además el concepto de especificidad absoluta, porque la enzima actúa en una sola clase de sustrato.

Otro modelo que explica la unión enzima sustrato es el modelo de encaje inducido, en donde el sustrato al combinarse con la enzima induce un cambio en la forma de esta, que es posible porque los sitios activos de la enzima son flexibles. El cambio de forma produce el ajuste optimo para la integración del sustrato con la enzima. Este modelo nos plantea otro tipo de especificidad, la relativa en donde la enzima se podrá combinar con más de una clase de sustrato, pero que son semejantes desde el punto de vista estructural.

La unión enzima-sustrato pone al sustrato en una proximidad y orientación óptimos que ahora pueden reaccionar y así se acelera la reacción. Al formarse nuevos enlaces el sustrato se convierte en producto. Este nuevo producto tiene escasa afinidad por la enzima por lo que se separa de ella. La enzima por su parte puede seguir catalizando la reacción de más moléculas de sustrato, para formar más moléculas de productos.
Las enzimas pueden actuar solas o requerir de un cofactor o una coenzima. El cofactor es generalmente un Ion metálico que aumenta la eficacia de la enzima sin ser indispensable para que actúe. En cambio la coenzima es una sustancia orgánica no proteica que es indispensable para la actividad enzimática.
Las coenzimas pueden estar íntima y permanentemente unidas a las proteínas, o bien unirse de forma débil y transitoria. Coenzimas importantes son, por ejemplo, el trifosfato de adenosina (ATP), él di nucleótido de nicotinamida y adenina (NAD), él di nucleótido fosfato de nicotinamida y adenina (NADP), la coenzima A, la UDP-glucosa, el grupo hemo de la hemoglobina y muchas vitaminas. Las coenzimas, junto con ciertos elementos químicos inorgánicos, reciben el nombre de cofactores enzimáticos. Algunas enzimas necesitan un cofactor inorgánico y otras un cofactor tipo coenzima. Algunas enzimas requieren cofactores de ambos tipos.
Las enzimas son regulables. De esta manera el producto final de una reacción es capaz de inhibir a la enzima cuando el producto está en una concentración suficiente para satisfacer una necesidad puntual. De no se así el producto no actúa sobre la ENZIMA Y ESTA ACTÚA SIN FRENO. Este Tipo de regulación se denomina por retroacción o retroalimentación.
REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA.
La velocidad de las reacciones enzimáticas puede ser modificada por diferentes factores, como: las concentraciones de sustrato, y la enzima, la inhibición o bloqueo de la actividad enzimática y la desnaturalización por temperatura, el pH o metales pesados.
Concentraciones: Si aumenta la concentración del sustrato o de la enzima, la velocidad de reacción también crece. O sea a más enzima o sustrato mayor es la cantidad de producto en un tiempo dado. A veces, algunas células pueden tener mucho sustrato y no poseer la enzima específica para ese sustrato. La enzima es entonces un factor limitante del metabolismo celular en esa célula.
Inhibición competitiva. Consiste en el bloqueo de la actividad enzimática por combinación de la enzima con otra molécula de estructura parecida a la del sustrato que se acomoda al sitio activo de la enzima e impide que ocurra la reacción normal. Este fenómeno se produce por ejemplo cuando ingresan a la célula sustancias tóxicas o venenos, donde estas sustancias compiten con la enzima uniéndose al sustrato pero en forma permanente impidiendo la generación de productos. Esto implica que el metabolismo celular cae a cero y la célula muere o se daña permanentemente.
Un ejemplo típico es la toxicidad hepática, que se produce en el hígado cuando este se satura por el consumo excesivo de medicamentos. Otro ejemplo es la acción del Curare que inhibe a las CoE en la respiración celular.
Desnaturalización: Las proteínas se desnaturalizan y dejan de funcionar. En el caso de las enzimas, tres factores ambientales pueden producir que las enzimas pierdan su funcionalidad por desnaturalización: la Tº , el pH, y metales pesados.
a) Temperatura: Las enzimas se inactivan con temperaturas altas, las reacciones enzimáticas ocurren lentamente o no se realizan a Tº menores a las de las células, pero la actividad catalítica reaparece cuando la Tº celular se aproxima a su normalidad. Tº superiores a 50º-60º C inactivar rápidamente a la mayoría de las enzimas porque el calor en exceso afecta los enlaces no covalentes de la molécula proteica, tales como los enlaces de H y causa su desnaturalización. Este cambio de la proteína es irreversible, la funcionalidad no se recupera cuando la enzima es enfriada.
b) pH. Las enzimas son sensibles a los cambios en la acidez o alcalinidad del medio en que actúa. Cada enzima exhibe un pH óptimo definido, que la capacita para desarrollar su actividad. El pH óptimo mantiene la funcionalidad de la enzima y su estructura proteica. Cuando el pH cambia la enzima pierde su forma normal y se desnaturaliza.
c) Metales pesados: Los iones de algunos metales pesados como el Pb. Y el Hg. precipitan a las proteínas e inactivan a las enzimas. Las enzimas están en suspensión en el citoplasma o unidas a una biomembrana. Si los iones de un metal pesado se combinan con una enzima en suspensión, las moléculas proteicas precipitan perdiendo su eficacia.
La fermentación alcohólica y otros procesos industriales importantes dependen de la acción de enzimas, sintetizadas por las levaduras y bacterias empleadas en el proceso de producción. Algunas enzimas se utilizan con fines médicos. En ocasiones son útiles en el tratamiento de zonas de inflamación local; la tripsina se emplea para eliminar sustancias extrañas y tejido muerto de las heridas y quemaduras.
El uso médico de las enzimas está ilustrado por la investigación sobre la L-asparaginasa, que se piensa es una herramienta importante para el tratamiento de la leucemia; se ha descubierto que las dextrinasas pueden prevenir la caída de los dientes, y que las alteraciones enzimáticas están ligadas a enfermedades como la fenilcetonuria, el albinismo, la diabetes, la anemia y otros trastornos sanguíneos.
ACTIVIDAD N° 2
1.- Explique de qué manera afecta a una enzima, la temperatura en los tres rangos : mínimo, óptimo y máximo
2.- A mayor concentración del substrato, la velocidad de la reacción aumenta, y alcanza cierto valor y se hace constante. Explica porque es importante este enunciado sobre las enzimas.
3.- El inhibidor sólo se une al complejo enzima - substrato, que ya no formará producto, por lo que la velocidad bajará. ¿Que efectos se pueden producir en una célula la acción de un inhibidor?
4.- Cual (es) de los siguientes factores afecta en la actividad enzimatica: Fundamenta
Las enzimas no se alteran ni se consumen, por lo que pueden volver a utilizarse
Cada enzima tiene uno o más sitios activos que se ubican en la superficie de la enzima. Durante la reacción las moléculas de sustrato que ocupan estos sitios quedan mas cerca unas de otras y reaccionan entre sí.
Se han propuesto dos modelos para explicar la unión enzima sustrato, según el modelo llave cerradura podría pensarse en las enzimas como una especie de cerradura molecular en donde entran solo llaves moleculares. Esta situación nos plantea además el concepto de especificidad absoluta, porque la enzima actúa en una sola clase de sustrato.
Otro modelo que explica la unión enzima sustrato es el modelo de encaje inducido, en donde el sustrato al combinarse con la enzima induce un cambio en la forma de esta, que es posible porque los sitios activos de la enzima son flexibles. El cambio de forma produce el ajuste optimo para la integración del sustrato con la enzima. Este modelo nos plantea otro tipo de especificidad, la relativa en donde la enzima se podrá combinar con más de una clase de sustrato, pero que son semejantes desde el punto de vista estructural.

La unión enzima-sustrato pone al sustrato en una proximidad y orientación óptimos que ahora pueden reaccionar y así se acelera la reacción. Al formarse nuevos enlaces el sustrato se convierte en producto. Este nuevo producto tiene escasa afinidad por la enzima por lo que se separa de ella. La enzima por su parte puede seguir catalizando la reacción de más moléculas de sustrato, para formar más moléculas de productos.
Las enzimas pueden actuar solas o requerir de un cofactor o una coenzima. El cofactor es generalmente un Ion metálico que aumenta la eficacia de la enzima sin ser indispensable para que actúe. En cambio la coenzima es una sustancia orgánica no proteica que es indispensable para la actividad enzimática.
Las coenzimas pueden estar íntima y permanentemente unidas a las proteínas, o bien unirse de forma débil y transitoria. Coenzimas importantes son, por ejemplo, el trifosfato de adenosina (ATP), él di nucleótido de nicotinamida y adenina (NAD), él di nucleótido fosfato de nicotinamida y adenina (NADP), la coenzima A, la UDP-glucosa, el grupo hemo de la hemoglobina y muchas vitaminas. Las coenzimas, junto con ciertos elementos químicos inorgánicos, reciben el nombre de cofactores enzimáticos. Algunas enzimas necesitan un cofactor inorgánico y otras un cofactor tipo coenzima. Algunas enzimas requieren cofactores de ambos tipos.
Las enzimas son regulables. De esta manera el producto final de una reacción es capaz de inhibir a la enzima cuando el producto está en una concentración suficiente para satisfacer una necesidad puntual. De no se así el producto no actúa sobre la ENZIMA Y ESTA ACTÚA SIN FRENO. Este Tipo de regulación se denomina por retroacción o retroalimentación.
REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA.
La velocidad de las reacciones enzimáticas puede ser modificada por diferentes factores, como: las concentraciones de sustrato, y la enzima, la inhibición o bloqueo de la actividad enzimática y la desnaturalización por temperatura, el pH o metales pesados.
Concentraciones: Si aumenta la concentración del sustrato o de la enzima, la velocidad de reacción también crece. O sea a más enzima o sustrato mayor es la cantidad de producto en un tiempo dado. A veces, algunas células pueden tener mucho sustrato y no poseer la enzima específica para ese sustrato. La enzima es entonces un factor limitante del metabolismo celular en esa célula.
Inhibición competitiva. Consiste en el bloqueo de la actividad enzimática por combinación de la enzima con otra molécula de estructura parecida a la del sustrato que se acomoda al sitio activo de la enzima e impide que ocurra la reacción normal. Este fenómeno se produce por ejemplo cuando ingresan a la célula sustancias tóxicas o venenos, donde estas sustancias compiten con la enzima uniéndose al sustrato pero en forma permanente impidiendo la generación de productos. Esto implica que el metabolismo celular cae a cero y la célula muere o se daña permanentemente.
Un ejemplo típico es la toxicidad hepática, que se produce en el hígado cuando este se satura por el consumo excesivo de medicamentos. Otro ejemplo es la acción del Curare que inhibe a las CoE en la respiración celular.
Desnaturalización: Las proteínas se desnaturalizan y dejan de funcionar. En el caso de las enzimas, tres factores ambientales pueden producir que las enzimas pierdan su funcionalidad por desnaturalización: la Tº , el pH, y metales pesados.
a) Temperatura: Las enzimas se inactivan con temperaturas altas, las reacciones enzimáticas ocurren lentamente o no se realizan a Tº menores a las de las células, pero la actividad catalítica reaparece cuando la Tº celular se aproxima a su normalidad. Tº superiores a 50º-60º C inactivar rápidamente a la mayoría de las enzimas porque el calor en exceso afecta los enlaces no covalentes de la molécula proteica, tales como los enlaces de H y causa su desnaturalización. Este cambio de la proteína es irreversible, la funcionalidad no se recupera cuando la enzima es enfriada.
b) pH. Las enzimas son sensibles a los cambios en la acidez o alcalinidad del medio en que actúa. Cada enzima exhibe un pH óptimo definido, que la capacita para desarrollar su actividad. El pH óptimo mantiene la funcionalidad de la enzima y su estructura proteica. Cuando el pH cambia la enzima pierde su forma normal y se desnaturaliza.
c) Metales pesados: Los iones de algunos metales pesados como el Pb. Y el Hg. precipitan a las proteínas e inactivan a las enzimas. Las enzimas están en suspensión en el citoplasma o unidas a una biomembrana. Si los iones de un metal pesado se combinan con una enzima en suspensión, las moléculas proteicas precipitan perdiendo su eficacia.
La fermentación alcohólica y otros procesos industriales importantes dependen de la acción de enzimas, sintetizadas por las levaduras y bacterias empleadas en el proceso de producción. Algunas enzimas se utilizan con fines médicos. En ocasiones son útiles en el tratamiento de zonas de inflamación local; la tripsina se emplea para eliminar sustancias extrañas y tejido muerto de las heridas y quemaduras.
El uso médico de las enzimas está ilustrado por la investigación sobre la L-asparaginasa, que se piensa es una herramienta importante para el tratamiento de la leucemia; se ha descubierto que las dextrinasas pueden prevenir la caída de los dientes, y que las alteraciones enzimáticas están ligadas a enfermedades como la fenilcetonuria, el albinismo, la diabetes, la anemia y otros trastornos sanguíneos.
ACTIVIDAD N° 2
1.- Explique de qué manera afecta a una enzima, la temperatura en los tres rangos : mínimo, óptimo y máximo
2.- A mayor concentración del substrato, la velocidad de la reacción aumenta, y alcanza cierto valor y se hace constante. Explica porque es importante este enunciado sobre las enzimas.
3.- El inhibidor sólo se une al complejo enzima - substrato, que ya no formará producto, por lo que la velocidad bajará. ¿Que efectos se pueden producir en una célula la acción de un inhibidor?
4.- Cual (es) de los siguientes factores afecta en la actividad enzimatica: Fundamenta
I.
temperatura II. pH III. Concentración del sustrato
UTILIZACION ENZIMATICA EN DIVERSAS AREAS
- Industrias lácteas:
1.- Para la elaboración de quesos se utiliza el cuajo
del estómago de las vacas, está formado por la mezcla de las enzimas: quimosina
y pepsina. Rompen la caseína de la leche y producen su coagulación.
2.- La enzima
lactasa rompe el azúcar de la leche llamada lactosa (la falta de la enzima
provoca trastornos intestinales).
Industrias Cerveceras:
1.-
Enzima papaína para romper proteínas presentes en la cerveza.(evita que se
enturbie).
2.-
Enzima bromelaína (piña).
3.-
Enzimas amilasas (presente en las las maltas) rompen enlaces almidón para luego
actuar la levadura.
Otros:
Fabricación
de glucosa y fructosa a partir del maíz
Una industria en franca expansión es la obtención de jarabes de glucosa o fructosa a partir de almidón de maíz. Estos jarabes se utilizan en la elaboración de bebidas refrescantes, conservas de frutas, repostería, etc. en lugar del azúcar de caña o de remolacha.
Una industria en franca expansión es la obtención de jarabes de glucosa o fructosa a partir de almidón de maíz. Estos jarabes se utilizan en la elaboración de bebidas refrescantes, conservas de frutas, repostería, etc. en lugar del azúcar de caña o de remolacha.
Actividad 3:
2.- ¿En qué lugar(es) de la célula se sintetizan las enzimas?, ¿cómo?
3.- De qué factores depende la acción enzimática? Explica.
4.- Construye o dibuja un gráfico que represente el efecto de la T° en la acción de las enzimas.
5.- ¿A qué se refiere la especificidad enzimática?, realiza un ejemplo.
6.- Investiga 3 enfermedades que se generen por acción defectuosa de las enzimas.
1.- ¿Cuál de los siguientes enunciados se aplican a Las enzimas?, ¿Porqué?:
I.
Son moléculas
formadas sólo por proteínas.
II. Están encargadas
de regular procesos anabólicos y catabólicos.
III.- Se modifican al final de la reacción2.- ¿En qué lugar(es) de la célula se sintetizan las enzimas?, ¿cómo?
3.- De qué factores depende la acción enzimática? Explica.
4.- Construye o dibuja un gráfico que represente el efecto de la T° en la acción de las enzimas.
5.- ¿A qué se refiere la especificidad enzimática?, realiza un ejemplo.
6.- Investiga 3 enfermedades que se generen por acción defectuosa de las enzimas.
Comentarios
Publicar un comentario